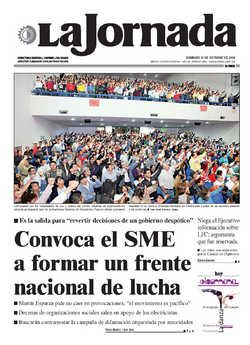
Anuncia Cofepris “ajustes” en el procedimiento; se dará más tiempo a laboratorios
Recibirán documentación a fabricantes aunque no hayan terminado pruebas de intercambiabilidad

Domingo 25 de octubre de 2009, p. 33
La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) realizará algunos “ajustes” en el proceso de renovación de los registros de medicamentos, a fin de que el próximo 24 de febrero, cuando vence el plazo para que los laboratorios inicien el trámite, puedan presentar la solicitud aun cuando su documentación esté incompleta.
Gustavo Olaiz, comisionado de Autorización Sanitaria del organismo, indicó que los fabricantes deberán presentar la evidencia sobre los avances que llevan en la acreditación de las pruebas de intercambiabilidad, con las cuales demostrarían que la calidad y eficacia terapéutica de sus productos es equivalente a la de los innovadores.
Indicó que a la fecha la Cofepris ha recibido las solicitudes de 80 por ciento de las medicinas que se venden en México y programa para las siguientes semanas otro 10 por ciento. Están pendientes mil 500 productos, sobre los cuales se desconoce si se renovarán sus registros sanitarios.
En cualquier caso, señaló el funcionario, si ahora concluyera el plazo, no faltaría ningún medicamento. Es decir, con los que ya han iniciado el trámite se garantiza el acceso a los fármacos necesarios para la atención de la totalidad de enfermedades que afectan a los mexicanos.
De acuerdo con la Ley General de Salud, a partir de 2010 todas las medicinas que se comercializan en el país deberán contar con las pruebas de intercambiabilidad, de tal suerte que sólo existirán innovadores (protegidos por una patente) y genéricos. Desaparecerá la figura de genérico intercambiable (GI) utilizada desde 1998 para aquellos productos que de manera voluntaria acreditaron ser equivalentes con los originales.
En adelante, los registros se renovarán cada cinco años y las nuevas fórmulas genéricas obtendrán el registro sólo con la evidencia de su calidad y eficacia terapéutica.
Olaiz participó en un foro organizado por la Asociación Mexicana de Fabricantes de Genéricos Intercambiables (Amegi), donde planteó los avances del proceso de renovación de los registros, el cual concluirá el 24 de febrero de 2010. Insistió en que no habrá prórroga alguna, aunque ahí mismo se escucharon las inquietudes de algunas empresas porque no lograrán tener a tiempo los resultados de las pruebas de intercambiabilidad de todas sus medicinas.
Algunos de los asistentes, representantes de laboratorios nacionales, comentaron que las pruebas son de alto costo –alrededor de 100 mil dólares–, situación que debería ser tomada en cuenta por la autoridad sanitaria, a fin de ampliar el plazo para la presentación de solicitudes de renovación de registros.
El presidente de Amegi, Rafael Enrique Maciel Martínez, resaltó que gran parte de los laboratorios empezaron desde 2002 con los procedimientos para realizar las pruebas de intercambiabilidad, cuando fue evidente la intención del gobierno federal de transformar el mercado a fin de que solamente existan innovadores y genéricos.
Reconoció, sin embargo, la importancia de ofrecer alternativas a las empresas que están retrasadas, “bajo ciertas condiciones”.
Sobre el tema, Olaiz explicó que habrá un “ajuste en los tiempos”, siempre que los laboratorios comprueben que están en el camino de realizar los exámenes de intercambiabilidad. La Cofepris estaría en condiciones de esperar los resultados de los estudios para después continuar con el trámite de la renovación del registro.